欄目導航 / navigation
證書查詢 / inquiry
體系證書編號:
產品證書編號:
聯絡我們 / contact

◆森維國際認證集團◆
◆Sanwei International Certification Ltd◆
電話 : +886-2-2918-1959
傳真 : +886-2-2918-1872
郵箱:sanwei.twn@gmail.com
品質: 專業 、 公平 、 公正
態度: 誠信 、 嚴謹 、 熱誠
FDA食品註冊
現在位置:公司官網 > FDA食品註冊
美國食品法規-保健食品分類
發布人: 點擊:1771次
保健食品的進出口貿易成為市場新興熱點,但同時各國對保健食品的定義、法規和監管體系都不盡相同。
1
美國食品分類及法規
1.6 保健食品分類
在美國,沒有保健食品類型。最接近保健食品分類的類別為食品補充物和醫療食品;這兩類食品是根據其功能進行劃分的。圖1顯示了美國的食品分類。
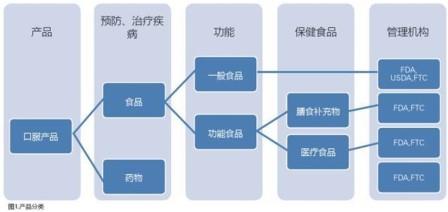
1.6.1膳食補充物
膳食補充物是按照《膳食補充物保健及教育法》(DSHEA)管理的。在1994年之前,膳食補充物需要遵守與其它食品一樣的管理要求。在1994年,美國國會在DSHEA中規定了“膳食補充物”的定義。
膳食補充物是一種口服產品,其中含有用來補充膳食的“膳食成分”。在這些產品中,“膳食成分”包括:維生素、礦物質、草藥、氨基酸以及酶、器官組織、腺體和代謝物等物質。
新膳食成分(NDI)指滿足上述膳食成分定義且在1994年10月15日之前未在美國出售過的膳食補充物。
DSHEA要求生產商或分銷商通知FDA其是否打算在美國出售含有柔佛巴魯石成分的膳食補充物。
在新膳食成分通知(NDIN)中,生產商(及分銷商)必須向FDA證明為何認為該成分在膳食補充物中可以安全使用,除非該成分被認定為食物成分且存在於食物的供應中。
在1994年10月15日之前出售的膳食成分沒有管理列表。因此,生產商和分銷商應負責確定某膳食成分是否是“新”的。
根據法律要求,生產商可為其膳食補充物產品提出三種成效:保健成效、結構/功能成效和營養成分成效。第3.2條列出了這些成效的更詳細的資訊。
FDA負責管理膳食補充物的貼標,包括標籤、包裝和附上的檔。聯邦貿易委員會(FTC)負責管理膳食補充物及大部分其他出售給消費者的產品。
1.6.2 醫療食品
醫療食品的定義在《孤兒藥物法》(21 U.S.C. 360ee(b)(3))第5(b)(3)條中。醫療食品是指在醫生監督下內服的食品,主要用於某病症或身體狀況的特定膳食管理,對此要按照認可的科學準則,通過醫療評估的方式確定獨特的營養要求。
添加到醫療食品中的成分必須是安全和適當的,且要符合所有相應的FD&C法律要求和FDA的規定。任何添加到醫療食品中的成分都應當是:
符合FDA的食品添加劑規定的食品添加劑(21CFR 172);
根據色素添加劑規定使用的色素添加劑(21 CFR 73與74);
有資質的專家廣泛認可的在規定使用條件下為安全的成分(一般認為安全,GRAS)(21 CFR 170.30及21 U.S.C. 321(s));
FDA發佈的提前批准授權的成分(21 CFR 170.3(l))。
醫療食品必須滿足所有的食品管理要求,例如:
當前良好生產實踐規定(21 CFR第110部分)
食品機構註冊規定(21CFR第1部分第H條)
密封容器中的熱加工低酸性食品規定(21 CFR 第113部分)
酸化食品規定(21 CFR 第114部分)
應急許可控制規定(21 CFR第108部分)
FDA的合規程序指導手冊確定了四大類醫療食品:
營養完整的產品
營養不完整的配方產品
口服補液產品
代謝紊亂配方產品(FDA, 1999)
有許多種類的產品被用於各種狀況的醫療管理,例如防止體重流失,從而為特殊人群提供適當的營養,並防止、控制及/或消除各種急性、遺傳和慢性疾病。
1.6.3 邊界產品
在膳食補充物和醫療食品之間存在一種“邊界產品”。如果某產品同時滿足食品和醫療產品的定義,則應當被認為是醫療產品,並據此進行管理。
醫療產品的安全性和效率必須通過大量的檔和臨床資訊來證明,然後才能進行註冊和上市。在另一方面,如果將某產品劃定為膳食補充物,則會限制對包裝材料的效果,尤其是保健效果。在對某產品進行戰略定位的時候,必須考慮這些管理要點。
1
美國食品分類及法規
1.6 保健食品分類
在美國,沒有保健食品類型。最接近保健食品分類的類別為食品補充物和醫療食品;這兩類食品是根據其功能進行劃分的。圖1顯示了美國的食品分類。

1.6.1膳食補充物
膳食補充物是按照《膳食補充物保健及教育法》(DSHEA)管理的。在1994年之前,膳食補充物需要遵守與其它食品一樣的管理要求。在1994年,美國國會在DSHEA中規定了“膳食補充物”的定義。
膳食補充物是一種口服產品,其中含有用來補充膳食的“膳食成分”。在這些產品中,“膳食成分”包括:維生素、礦物質、草藥、氨基酸以及酶、器官組織、腺體和代謝物等物質。
新膳食成分(NDI)指滿足上述膳食成分定義且在1994年10月15日之前未在美國出售過的膳食補充物。
DSHEA要求生產商或分銷商通知FDA其是否打算在美國出售含有柔佛巴魯石成分的膳食補充物。
在新膳食成分通知(NDIN)中,生產商(及分銷商)必須向FDA證明為何認為該成分在膳食補充物中可以安全使用,除非該成分被認定為食物成分且存在於食物的供應中。
在1994年10月15日之前出售的膳食成分沒有管理列表。因此,生產商和分銷商應負責確定某膳食成分是否是“新”的。
根據法律要求,生產商可為其膳食補充物產品提出三種成效:保健成效、結構/功能成效和營養成分成效。第3.2條列出了這些成效的更詳細的資訊。
FDA負責管理膳食補充物的貼標,包括標籤、包裝和附上的檔。聯邦貿易委員會(FTC)負責管理膳食補充物及大部分其他出售給消費者的產品。
1.6.2 醫療食品
醫療食品的定義在《孤兒藥物法》(21 U.S.C. 360ee(b)(3))第5(b)(3)條中。醫療食品是指在醫生監督下內服的食品,主要用於某病症或身體狀況的特定膳食管理,對此要按照認可的科學準則,通過醫療評估的方式確定獨特的營養要求。
添加到醫療食品中的成分必須是安全和適當的,且要符合所有相應的FD&C法律要求和FDA的規定。任何添加到醫療食品中的成分都應當是:
符合FDA的食品添加劑規定的食品添加劑(21CFR 172);
根據色素添加劑規定使用的色素添加劑(21 CFR 73與74);
有資質的專家廣泛認可的在規定使用條件下為安全的成分(一般認為安全,GRAS)(21 CFR 170.30及21 U.S.C. 321(s));
FDA發佈的提前批准授權的成分(21 CFR 170.3(l))。
醫療食品必須滿足所有的食品管理要求,例如:
當前良好生產實踐規定(21 CFR第110部分)
食品機構註冊規定(21CFR第1部分第H條)
密封容器中的熱加工低酸性食品規定(21 CFR 第113部分)
酸化食品規定(21 CFR 第114部分)
應急許可控制規定(21 CFR第108部分)
FDA的合規程序指導手冊確定了四大類醫療食品:
營養完整的產品
營養不完整的配方產品
口服補液產品
代謝紊亂配方產品(FDA, 1999)
有許多種類的產品被用於各種狀況的醫療管理,例如防止體重流失,從而為特殊人群提供適當的營養,並防止、控制及/或消除各種急性、遺傳和慢性疾病。
1.6.3 邊界產品
在膳食補充物和醫療食品之間存在一種“邊界產品”。如果某產品同時滿足食品和醫療產品的定義,則應當被認為是醫療產品,並據此進行管理。
醫療產品的安全性和效率必須通過大量的檔和臨床資訊來證明,然後才能進行註冊和上市。在另一方面,如果將某產品劃定為膳食補充物,則會限制對包裝材料的效果,尤其是保健效果。在對某產品進行戰略定位的時候,必須考慮這些管理要點。


